- Accueil >
- Les actualités de l'Institut Curie >
- Shadocks et embryons, même combat
Le lumen de l’embryon se forme à partir de centaines de mini-lumens
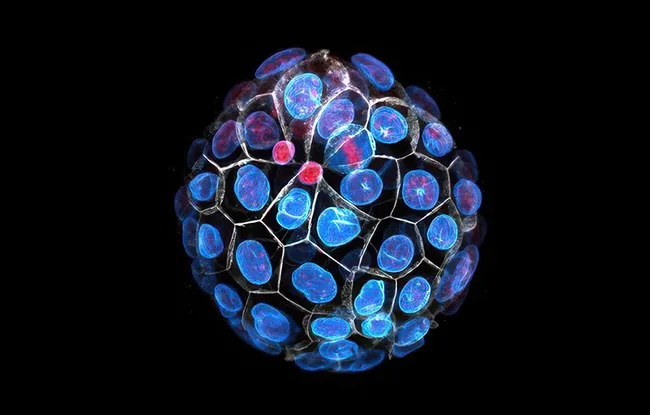
Cerveau, cœur, foie, reins, la plupart des organes de notre corps contiennent des cavités remplies de fluide. Ces cavités appelées lumens sont essentielles au bon fonctionnement de nos organes. Durant les tous premiers jours de notre développement, alors qu’il ne consiste que de 32 cellules, l’embryon forme son premier lumen. Ce lumen gonfle à l’intérieur de l’embryon et sa position détermine l’endroit par lequel l’embryon s’attachera à l’utérus maternel pour s’implanter et continuer son développement.
En 2019, une étude dirigée par le Dr Jean-Léon Maître, chef de l’équipe Mécanique du développement des mammifères (CNRS UMR3215 / Inserm U934 / Sorbonne Université), avait montré que le lumen se forme par fracturation hydraulique : la pression du fluide brise les contacts entre les cellules. Mais cette fracturation ne forme pas un seul lumen mais des centaines de mini-lumens, ou poches, qui progressivement échangent leur contenu et se vident les uns dans les autres jusqu'à ce qu’un seul lumen dominant accumule tout le fluide. Ainsi, ces écoulements entre poches sont cruciaux pour positionner le lumen et déterminer le point d’implantation. Mais comment les cellules contrôlent elles les mouvements du fluide au sein de l’embryon ?
Des milliers de pompes, les blebs inversés, pour assurer la formation du lumen
Dans un article publié dans la revue Nature Cell Biology, les mêmes scientifiques ont découvert des structures appelées blebs inversés qui pompent le fluide d’une poche vers l’autre. Ces blebs inversés se gonflent de fluide en 10 secondes pour atteindre quelques micromètres de diamètres avant de se contracter en 30 secondes pour repousser le fluide. Pour passer d’un réseau de poches à un seul gros lumen en quelques heures, ce sont des milliers et des milliers de blebs inversés qui apparaissent et disparaissent au sein de chaque embryon.
En manipulant la capacite des embryons à accumuler du fluide ou à contraindre le fluide dans les poches, les scientifiques ont montré que les blebs inversés se forment grâce à la pression du fluide qui pousse comme un ballon vers l’intérieur des cellules. Celles-ci recrutent rapidement des protéines du cytosquelette d’actomyosine (les mêmes qui permettent à nos muscles de se contracter) a la surface des blebs inversés et repoussent le fluide vers d’autres poches. Ainsi, les blebs inversés pompent et pompent et pompent encore le fluide au sein de l’embryon, le faisant ainsi circuler. Mais ce va-et-vient du fluide ne semble pas très productif.
Les scientifiques ont alors identifié que certaines poches, celles entourées par plus de deux cellules, ne formaient pas de blebs inversés avec une fréquence aussi élevée que les autres poches contenant seulement deux cellules. En fait, les poches entourées par plus de deux cellules ne pomperaient pas efficacement et agiraient comme un syphon. Pour étayer cette hypothèse, les scientifiques ont manipulé la topologie des embryons de façon à éliminer les poches entourées par plus de deux cellules. Ces structures dépourvues de siphon forment énormément de blebs inversés mais, comme ils pompent le fluide de l’un vers l’autre dans un cycle futile, elles ne parviennent que péniblement à former un lumen. Ainsi, ces structures sans siphon sont à l’image des Shadocks dont un des adages est "Il vaut mieux pomper et qu'il ne se passe rien plutôt que de ne pas pomper et risquer qu'il se passe quelque chose de pire”.
Cette étude met donc en lumière les blebs inversés comme le mécanisme cellulaire permettant aux embryons de former un seul lumen dont la position détermine son futur développement. Elle révèle également que pour dépasser les premiers jours du développement de l’embryon de mammifère il est essentiel de suivre cette autre maxime Shadockienne : « je pompe donc je suis ».
Schliffka, M.F., Dumortier, J.G., Pelzer, D. et al. Inverse blebs operate as hydraulic pumps during mouse blastocyst formation. Nat Cell Biol (2024). https://doi.org/10.1038/s41556-024-01501-z

Schéma de la formation du lumen de l’embryon de souris. Du fluide (bleu) s’accumule entre les cellules à l’intérieur de l’embryon. Les poches remplies de fluides échangent leur contenu jusqu'à ce qu’il ne reste qu’une seule poche et constitue le lumen qui détermine l’axe de symétrie de l’embryon et son point d’implantation. Pour aider les poches à échanger le fluide, des structures appelées blebs inversés (vert) pompent le fluide d’une poche vers l’autre.