- Accueil >
- Liste Annuaire >
- ANNE HOUDUSSE-JUILLE
Fonctions au sein de l’Institut Curie
Chef d'équipe de recherche
Équipe :
Motilité structuralePrésentation
Anne Houdusse, Ph.D. est directrice de recherche au CNRS, responsable de l’équipe Motilité Structurale du laboratoire Biologie cellulaire et cancer (CNRS/Institut Curie). En intégrant l’Ecole Normale Supérieure ULM, Anne Houdusse a choisi une formation de chimiste (Agrégation en 1989) avec une spécialité en biologie structurale. Après un doctorat effectué à l’Institut Pasteur obtenu en 1992, Anne Houdusse a reçu une bourse EMBO suivie d’une bourse HFSPO pour étudier la contraction musculaire à l'Université Brandeis (Waltham, MA, USA) avec les Drs. Carolyn Cohen et Andrew Szent Györgyi. Son projet ATIP a été sélectionné en 1999, permettant l’étude du cytosquelette et des moteurs cellulaires essentiels. En choisissant l’Institut Curie pour installer son laboratoire indépendant ‘Motilité Structurale’, Anne Houdusse a mis en place la biologie structurale à l’Institut Curie en 1999 de façon à faciliter l’étude de questions de biologie cellulaire et de maladies humaines, telles que le cancer.
Anne Houdusse a reçu les médailles de bronze et d'argent du CNRS et elle a été élue membre de l'EMBO en 2013. Elle a été récompensée par un prix FEBS pour ses réalisations exceptionnelles dans le domaine de la biologie structurale en 2005. Ses découvertes sur les nanomoteurs lui ont permis de recevoir le prix FEBS/EMBO Women in Science Award en 2009 et le Prix Lecocq de l'Académie française des sciences en 2018. Elle a été élue membre de l'Académie française des sciences (Institut de France) en décembre 2019.
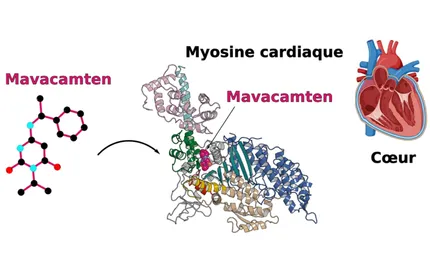
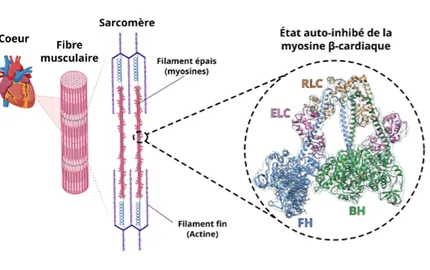
Le laboratoire d’Anne Houdusse étudie les nanomachines, ces moteurs moléculaires qui produisent une force au sein de nos cellules, et qui sont essentiels pour leur organisation dynamique, leurs capacités à se contracter et à migrer. À partir des connaissances structurales à haute résolution, le défi réside à identifier le rôle précis joué par chacun de ces moteurs lorsqu’ils participent à une fonction cellulaire de manière coordonnée. La plupart sont également impliqués dans de nombreuses pathologies ; comprendre comment contrôler leur activité ouvre la voie vers de nouvelles solutions thérapeutiques.
Dernières publications
The European Physical Journal E - 01/09/2025
Cell - 01/08/2025
The EMBO Journal - 27/08/2024
Dernière actualité
Contacter ANNE HOUDUSSE-JUILLE
Contactez-moi en renseignant le formulaire ci-dessous