- Accueil >
- Les actualités de l'Institut Curie >
- L’immunothérapie, un nouvel allié contre le cancer du col de l’utérus ?
Le cancer du col de l’utérus est la deuxième cause de mortalité par cancer dans le monde chez les femmes de 20 à 39 ans. Lorsqu’il est localement avancé, le traitement standard consiste à allier chimiothérapie et radiothérapie, mais les patientes restent exposées à un risque de récidive de 40 %.
Notre ambition est de trouver des combinaisons de traitements plus efficaces
Annonce le Dr Emanuela Romano, directrice médicale du Centre d’immunothérapie des cancers de l’Institut Curie.
C’est ainsi qu’avec une équipe de chercheurs, oncologues, radiothérapeutes et chirurgiens, le Dr Manuel Rodrigues, oncologue médical et chercheur dans l’équipe Réparation de l’ADN et mélanome uvéal (D.R.U.M) (Inserm U830), et le Dr Emanuela Romano se sont intéressés à l’alliance de ce traitement classique à une immunothérapie. Cette dernière consiste à cibler la réponse immunitaire – ou, plus exactement, son inhibition. Celle-ci existe en effet naturellement dans le corps humain : des points de contrôle sur les cellules tumorales peuvent limiter la réponse immunitaire. Or les cellules tumorales abusent de ce processus afin d’échapper au système immunitaire.
Réussir à inhiber… l’inhibition
L’idée des chercheurs ? Inhiber ces points de contrôle pour que la tumeur ne puisse plus éviter la réponse immunitaire. Les Drs Romano et Rodrigues et leurs collègues ont ainsi testé chez 16 patientes atteintes d’un cancer du col de l’utérus localement avancé la combinaison de la chimioradiothérapie avec une immunothérapie via le nivolumab, un inhibiteur des points de contrôle.
L’objectif premier était de vérifier la tolérance et la sécurité de ce traitement
Précisent les médecins.
Et celui-ci a été rempli : la dose de 240 mg de nivolumab, administrée toutes les deux semaines pendant les cinq semaines de chimioradiothérapie puis durant les six mois suivants, n’a provoqué aucun effet secondaire grave.
Les lymphocytes T : des biomarqueurs potentiels
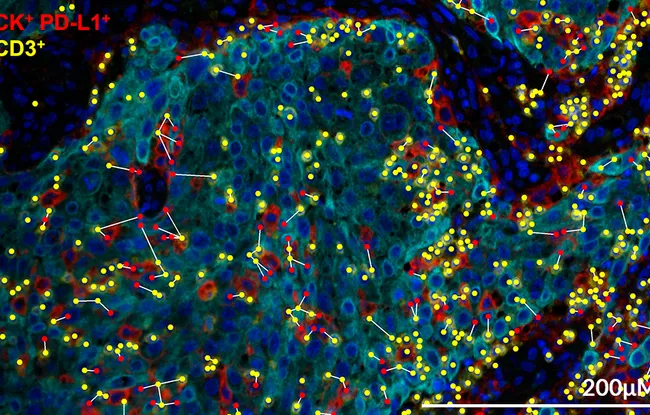
Ces recherches ont en outre apporté une deuxième bonne nouvelle : elles ont révélé des biomarqueurs potentiellement prédictifs de l’efficacité de ce nouveau traitement. Les chercheurs ont en effet observé que les patientes y ayant le mieux répondu étaient celles qui présentaient au départ plus de lymphocytes T déjà présent dans la tumeur et de molécules de co-stimulation.
C’est le signe que leur système immunitaire s’est déjà attaqué au cancer. Et le nivolumab aide à soutenir cette réponse.
Note le Dr Giulia Vanoni, chercheuse post-doctorant dans l’équipe Réponses immunitaires et cancer (Inserm U932), particulièrement impliquée dans les études de laboratoire.
A l’inverse, les patientes ayant mal répondu présentaient davantage de lymphocytes régulateurs, signe d’une immunosuppression systémique.
Sélectionner les patientes correspondant au premier profil permettrait de mettre en place un essai clinique destiné à juger cette fois l’efficacité de cette nouvelle combinaison. Dans cette première étude, elle est sensiblement identique à celle obtenue avec une chimioradiothérapie seule (un taux de survie sans progression à deux ans de 75 %), « mais l’échantillon est trop petit pour être représentatif », souligne le Dr Romano.
En attendant cette prochaine étape, les médecins et chercheurs de l’Institut Curie maintiennent leur travail de suivi de leurs patientes : la durée de survie sans récidive à long terme sera elle aussi un indicateur en faveur, ou non, d’une éventuelle intégration du nivolumab dans l’arsenal thérapeutique.